Gaz yasaları, gazlardaki termodinamik sıcaklık (T), basınç (P) ve hacim (V) aralarındaki ilişkileri açıklayan bir takım kanundur. Rönesans'ın geç dönemleriyle 19. yüzyıl arasındaki dönemde bulunmuş birkaç yasadan oluşur.
İdeal gazlar
En baştaki gaz yasaları
Boyle yasası (1662),
Charles yasası (1787-1802)
Gay-Lussac yasası (1809)
birleşip, toplam gaz yasasını oluştururlar:
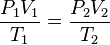
Daha sonra Avogadro yasasının da eklenmesiyle ideal gaz yasası oluşmuştur:
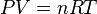
P paskal olarak basınç,
V kübik metre olarak hacim,
n gazın mol sayısı,
R gaz sabiti (8.3145 J/(mol K))
T de Kelvin olarak sıcaklıktır.
(Yukardakiler SI birimleridir. Yasa, her birimle çalışmaktadır, ancak gaz sabiti buna göre çevrilmeli ve sıcaklığın da mutlak sıfırda tam sıfır olduğu bir sistem kullanılmalıdır)
Diğer önemli gaz yasaları olan Dalton yasası, kinetik teori ve Graham yasası da gazların basınç, hacim ve sıcaklığa göre nasıl davrandıklarını açıklar.
Bu yasaların tamı tamına geçerli olduğu tüm gazlara, ideal gaz denir. İdeal bir gaz yoktur ancak bazı gazlar, bu yasalara daha çok uyabilir.
İdeal gazlar
En baştaki gaz yasaları
Boyle yasası (1662),
Charles yasası (1787-1802)
Gay-Lussac yasası (1809)
birleşip, toplam gaz yasasını oluştururlar:
Daha sonra Avogadro yasasının da eklenmesiyle ideal gaz yasası oluşmuştur:
P paskal olarak basınç,
V kübik metre olarak hacim,
n gazın mol sayısı,
R gaz sabiti (8.3145 J/(mol K))
T de Kelvin olarak sıcaklıktır.
(Yukardakiler SI birimleridir. Yasa, her birimle çalışmaktadır, ancak gaz sabiti buna göre çevrilmeli ve sıcaklığın da mutlak sıfırda tam sıfır olduğu bir sistem kullanılmalıdır)
Diğer önemli gaz yasaları olan Dalton yasası, kinetik teori ve Graham yasası da gazların basınç, hacim ve sıcaklığa göre nasıl davrandıklarını açıklar.
Bu yasaların tamı tamına geçerli olduğu tüm gazlara, ideal gaz denir. İdeal bir gaz yoktur ancak bazı gazlar, bu yasalara daha çok uyabilir.




 mujaxxx
mujaxxx