ELEKTRON DAĞILIMI
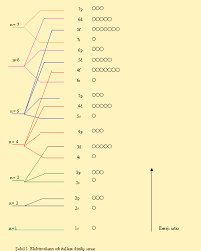
Atomun çekirdeği etrafında elektronların dizildiği yörünge adını verdiğimiz enerji katmanları vardır. Çekirdeğin etrafından başlayarak 1.2.3.4..... yörünge şeklinde sıralanırlar. Her yörüngede bulunacak elektron sayısı ise 2n2 ile hesaplanır.
n = yörünge sayısıdır.
1.yörünge = 2 2.yörünge = 8 3.yörünge = 18 4.yörünge = 32 Dış yörüngedeki elektronlar kolayca atomdan ayrılabilir. İlk yörüngedeki elektronlar kolayca ayrılamaz. Son yörüngede en fazla 8 bir önceki yörüngesinde ise en fazla 18 elektron bulunur. Atomlar son yörüngelerini ya 8 ya da 2 ye tamamlamak ister. Böylece soygaza benzemek ister. (okted-dukted kuralı) Hidrojen = 1
Neon = 2 8
Potasyum = 2 8 8 1
Helyum = 2
Sodyum = 2 8 1
Kalsiyum = 2 8 8 2
Lityum = 2 1
Magnezyum= 2 8 2
Berilyum = 2 2
Alüminyum= 2 8 3
Bor = 2 3
Silisyum = 2 8 4
Karbon = 2 4
Fosfor = 2 8 5
Azot = 2 5
Kükürt = 2 8 6
Oksijen = 2 6
Klor = 2 8 7
Flor = 2 7
Argon = 2 8 8
NOT: Son yörüngesinde 1 , 2 veya 3 elektron bulunan elementler ****ldir.
Son yörüngesinde 4 , 5 ,6 veya 7 elektron bulunduran elementler a****ldir.
Son yörüngesinde 8 elektron bulunduran elementler soygazdır.
ATOMLAR ARASI BAĞLAR
Atomları bir arada tutan kuvvetlere kimyasal bağ adı verilir. Tuğla arasına konan harç gibi. İyonik ve Kovalent bağ olmak üzere iki çeşittir.
İYONİK BAĞ : ****l ve a****l atomlarının bir araya gelmesiyle oluşur. A****l elektron alarak (-) , ****l ise elektron vererek (+) elektrikle yüklenir. Bu şekilde elektrikle yüklü atomlara İYON denir. Bu şekildeki elektron alışverişine ise İYONİK BAĞ veya Elektriksel Çekim Kuvveti denir.
ÖRNEK : NaCl , LiF , MgCl , CaCl2 , CaO vb.
KOVALENT BAĞ : İki a****l atomunun bir araya gelip karşılıklı olarak birbirlerinin elektronlarını ortak kullanmasıyla oluşan bağa Kovalent Bağ denir. Her iki a****lde elektron alarak (-) yüklenmek ister. Bu nedenle elektron çiftlerini ortak kullanırlar.
ÖRNEK : H2 , Cl2 , N2 , O2 , F2 , NH3 ,H2O
İYON NEDİR ? : Elektrikle yüklü atom veya atom gruplarına İYON denir.
ÖRNEK: Aşağıdaki bileşiklerin kimyasal bağlarının türünü söyleyiniz?
[ Na : 11 ; CI : 17 ; C : 6 ; O : 8
Mg : 12 ; F : 9 ; H : 1 ]
A-) NaCI B-) CO2 C-) MgF2 D-) H2O
Cevap:
A-) Na : 2 . 8 . 1 -----> ****l CI : 2 . 8 . 7 --- > a****l ****l--a****l arasında iyonik bağ vardır.
B-) C : 2 . 4 ------> a****l O : 2 . 6 ----> a****l a****l –a****l arasında kovalent bağ vardır.
C-) Mg: 2 . 8 . 2 ----> ****l F : 2 . 7 ----> a****l ****l –a****l arasında iyonik bağ vardır.
D-) H : 1 ------> a****l O : 2 . 6 ----> a****l a****l –a****l arasında kovalent bağ vardır.
NOT : Hidrojenin son yörüngesinde bir elektron olmasına rağmen a****l özelliği gösterir.
SORULAR:
1- İyonik bağ nasıl gerçekleşir ?
2- Kovalent bağ nasıl gerçekleşir ?
3- Kimyasal bağ nedir ?
4- Elektronlar hangi yörüngede en zayıftır ?
5- Elektronlar hani durumda yörüngeden kopmaz ?
Atomun çekirdeği etrafında elektronların dizildiği yörünge adını verdiğimiz enerji katmanları vardır. Çekirdeğin etrafından başlayarak 1.2.3.4..... yörünge şeklinde sıralanırlar. Her yörüngede bulunacak elektron sayısı ise 2n2 ile hesaplanır.
n = yörünge sayısıdır.
1.yörünge = 2 2.yörünge = 8 3.yörünge = 18 4.yörünge = 32 Dış yörüngedeki elektronlar kolayca atomdan ayrılabilir. İlk yörüngedeki elektronlar kolayca ayrılamaz. Son yörüngede en fazla 8 bir önceki yörüngesinde ise en fazla 18 elektron bulunur. Atomlar son yörüngelerini ya 8 ya da 2 ye tamamlamak ister. Böylece soygaza benzemek ister. (okted-dukted kuralı) Hidrojen = 1
Neon = 2 8
Potasyum = 2 8 8 1
Helyum = 2
Sodyum = 2 8 1
Kalsiyum = 2 8 8 2
Lityum = 2 1
Magnezyum= 2 8 2
Berilyum = 2 2
Alüminyum= 2 8 3
Bor = 2 3
Silisyum = 2 8 4
Karbon = 2 4
Fosfor = 2 8 5
Azot = 2 5
Kükürt = 2 8 6
Oksijen = 2 6
Klor = 2 8 7
Flor = 2 7
Argon = 2 8 8
NOT: Son yörüngesinde 1 , 2 veya 3 elektron bulunan elementler ****ldir.
Son yörüngesinde 4 , 5 ,6 veya 7 elektron bulunduran elementler a****ldir.
Son yörüngesinde 8 elektron bulunduran elementler soygazdır.
ATOMLAR ARASI BAĞLAR
Atomları bir arada tutan kuvvetlere kimyasal bağ adı verilir. Tuğla arasına konan harç gibi. İyonik ve Kovalent bağ olmak üzere iki çeşittir.
İYONİK BAĞ : ****l ve a****l atomlarının bir araya gelmesiyle oluşur. A****l elektron alarak (-) , ****l ise elektron vererek (+) elektrikle yüklenir. Bu şekilde elektrikle yüklü atomlara İYON denir. Bu şekildeki elektron alışverişine ise İYONİK BAĞ veya Elektriksel Çekim Kuvveti denir.
ÖRNEK : NaCl , LiF , MgCl , CaCl2 , CaO vb.
KOVALENT BAĞ : İki a****l atomunun bir araya gelip karşılıklı olarak birbirlerinin elektronlarını ortak kullanmasıyla oluşan bağa Kovalent Bağ denir. Her iki a****lde elektron alarak (-) yüklenmek ister. Bu nedenle elektron çiftlerini ortak kullanırlar.
ÖRNEK : H2 , Cl2 , N2 , O2 , F2 , NH3 ,H2O
İYON NEDİR ? : Elektrikle yüklü atom veya atom gruplarına İYON denir.
ÖRNEK: Aşağıdaki bileşiklerin kimyasal bağlarının türünü söyleyiniz?
[ Na : 11 ; CI : 17 ; C : 6 ; O : 8
Mg : 12 ; F : 9 ; H : 1 ]
A-) NaCI B-) CO2 C-) MgF2 D-) H2O
Cevap:
A-) Na : 2 . 8 . 1 -----> ****l CI : 2 . 8 . 7 --- > a****l ****l--a****l arasında iyonik bağ vardır.
B-) C : 2 . 4 ------> a****l O : 2 . 6 ----> a****l a****l –a****l arasında kovalent bağ vardır.
C-) Mg: 2 . 8 . 2 ----> ****l F : 2 . 7 ----> a****l ****l –a****l arasında iyonik bağ vardır.
D-) H : 1 ------> a****l O : 2 . 6 ----> a****l a****l –a****l arasında kovalent bağ vardır.
NOT : Hidrojenin son yörüngesinde bir elektron olmasına rağmen a****l özelliği gösterir.
SORULAR:
1- İyonik bağ nasıl gerçekleşir ?
2- Kovalent bağ nasıl gerçekleşir ?
3- Kimyasal bağ nedir ?
4- Elektronlar hangi yörüngede en zayıftır ?
5- Elektronlar hani durumda yörüngeden kopmaz ?
